合作客戶/
拜耳公司 |
同濟(jì)大學(xué) |
聯(lián)合大學(xué) |
美國(guó)保潔 |
美國(guó)強(qiáng)生 |
瑞士羅氏 |
相關(guān)新聞Info
推薦新聞Info
-
> 泡沫酸液表面張力調(diào)控與無(wú)機(jī)礦物溶蝕解堵特性研究(三)
> 泡沫酸液表面張力調(diào)控與無(wú)機(jī)礦物溶蝕解堵特性研究(二)
> 泡沫酸液表面張力調(diào)控與無(wú)機(jī)礦物溶蝕解堵特性研究(一)
> 烷基化碳量子點(diǎn)表面活性劑合成改性、表面張力、穩(wěn)泡及乳化性能(三)
> 烷基化碳量子點(diǎn)表面活性劑合成改性、表面張力、穩(wěn)泡及乳化性能(二)
> 烷基化碳量子點(diǎn)表面活性劑合成改性、表面張力、穩(wěn)泡及乳化性能(一)
> pH調(diào)控豬血漿蛋白納米顆粒的界面吸附行為與乳液穩(wěn)定機(jī)制(五)
> pH調(diào)控豬血漿蛋白納米顆粒的界面吸附行為與乳液穩(wěn)定機(jī)制(四)
> pH調(diào)控下豬血漿蛋白熱誘導(dǎo)納米顆粒的制備、表征及其穩(wěn)定Pickering乳液性能(三)
> pH調(diào)控下豬血漿蛋白熱誘導(dǎo)納米顆粒的制備、表征及其穩(wěn)定Pickering乳液性能(二)
表面張力自由能的分子論含義
來(lái)源:知乎 阿黃sweetgirl 瀏覽 1901 次 發(fā)布時(shí)間:2021-08-21
毛細(xì)作用的尺度在微米到毫米之間,其所處的尺度是連接宏觀與微觀的橋梁。表面張力不但與表面化學(xué)性質(zhì)(分子層次)有關(guān),還與宏觀的現(xiàn)象,比如毛細(xì)浸潤(rùn),毛細(xì)上升等現(xiàn)象有關(guān)。從分子層次上去理解表面能,表面張力的概念,對(duì)界面的微觀認(rèn)識(shí)具有重要的意義。

下面我們從分子論的角度來(lái)認(rèn)識(shí)表面自由能。
表面自由能定義為“將本體沿某一界面分開(kāi)克服本體內(nèi)分子間內(nèi)聚引力的作用所需要做的可逆功”。這種克服內(nèi)聚引力所做的功以勢(shì)能的形式儲(chǔ)存在新產(chǎn)生的表面上,就是表面自由能。
按照分子理論,兩個(gè)分子間存在Van der Waals力,對(duì)應(yīng)存在兩分子間的van der Waals相互作用勢(shì),其表達(dá)式為
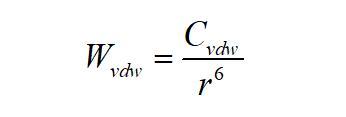
式中,Cvdw為Van der Waals分子對(duì)作用勢(shì)系數(shù),且
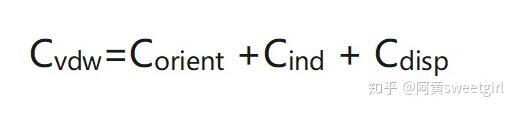
其中,Corient為Kessom分子對(duì)取向作用勢(shì)系數(shù),Cind為Debye分子對(duì)誘導(dǎo)作用勢(shì)系數(shù),Cdisp為L(zhǎng)ondon分子對(duì)色散作用勢(shì)系數(shù)。為分子方便,把原公式中負(fù)號(hào)去掉,即把吸引作用是為正。
而兩分子間的Van der Waals力的大小和表示為:
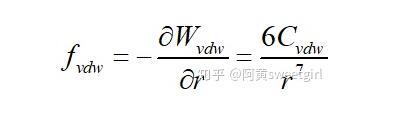
其方向沿兩分子的連線方向。
對(duì)于物體系統(tǒng)來(lái)說(shuō),按照Hamaker理論,物體系統(tǒng)的總作用勢(shì)等于各個(gè)分子間互相作用勢(shì)的疊加,即
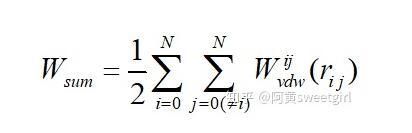
式中Wij是分子i和分子j間的不受其他分子影響的互作用勢(shì);rij是分子i和分子j間的距離;N為總分子數(shù)。
根據(jù)這一原理,單個(gè)分子與有限厚無(wú)限大平板的互作用勢(shì)為
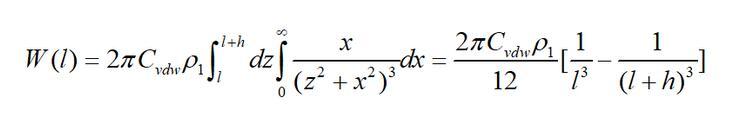
始終ρ1為無(wú)限大平板物體單位體積的分子數(shù)(分子密度);h為平板的厚度;l為單個(gè)分子到平板的最近距離。
當(dāng)厚度取無(wú)限大時(shí)可得單個(gè)分子與半無(wú)限體間的互作用勢(shì)為
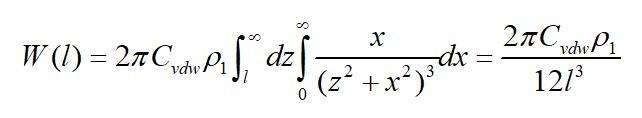
將單個(gè)分子換成有限厚無(wú)限大平板的單位面積,可得有限厚無(wú)限大平板之間的互作用勢(shì)為
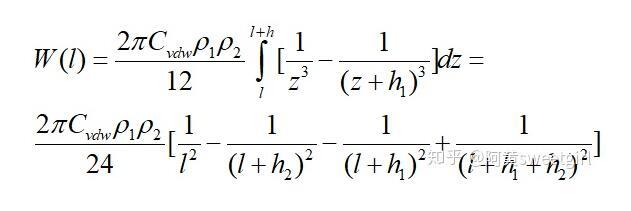
式子中h1和h2分別為兩無(wú)限大平板的厚度。
當(dāng)h1趨近于無(wú)窮時(shí),得有限厚無(wú)限大平板與半無(wú)限體的互作用勢(shì)為
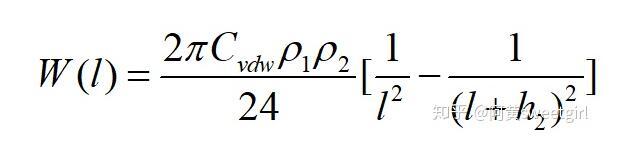
當(dāng)h1和h2都趨近于無(wú)窮時(shí),得兩半無(wú)限體之間的互作用勢(shì)為
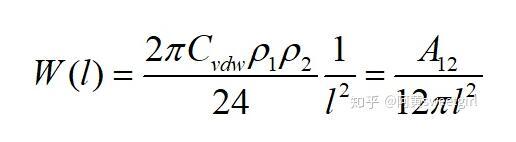
式中A12為Hamaker常數(shù)。定義為:
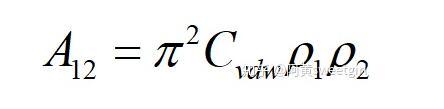
若取l為物質(zhì)本體內(nèi)分子間的距離d11,且兩半無(wú)限體為同一種物質(zhì)時(shí),則上式的互作用勢(shì)變?yōu)椋ㄈ〗^對(duì)值
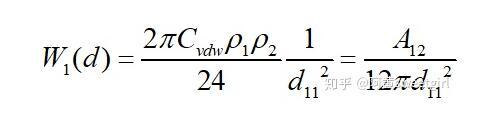
式中,

為物質(zhì)1的Hamaker常數(shù)。該作用勢(shì)能就相當(dāng)于本體的內(nèi)聚功。從表面自由能的定義不難看出,當(dāng)將本體沿本體內(nèi)的一個(gè)界面分開(kāi)時(shí),單位面積需要克服內(nèi)聚力所做的功就等于這個(gè)作用勢(shì)能。由于分開(kāi)后形成兩個(gè)新表面,因此每個(gè)表面上的勢(shì)能等于該勢(shì)能的一半。因此物體的表面自由能(表面張力)也等于該作用勢(shì)能的一半,即
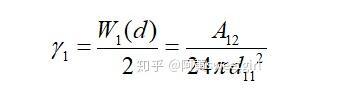
同樣,若取l為兩相界面處分子間的距離d12,且兩半無(wú)限體為兩種不同的物質(zhì)時(shí),則互作用勢(shì)變?yōu)?
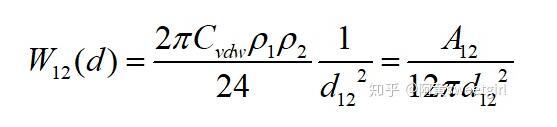
該作用勢(shì)能就相當(dāng)于兩相之間的粘附功。由于粘附功與表面張力(自由能)和界面張力(自由能)有如下關(guān)系:
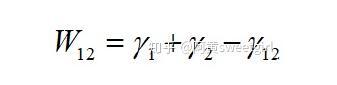
式中γ12為界面張力(自由能)。則界面張力/自由能可表示為:
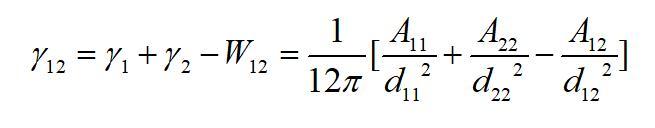
式中d11為物質(zhì)1的分子間距;d22為物質(zhì)2的分子間距;d12為物質(zhì)1和物質(zhì)2在界面處的分子間距;A11、A22及A12分別為物質(zhì)1本體內(nèi)、物質(zhì)2本體內(nèi)及物質(zhì)1與物質(zhì)2之間的Hamaker常數(shù)。
參考:節(jié)選自《毛細(xì)力學(xué)》第三章,高世橋,劉海鵬,科學(xué)出版社,2010.










